|
Ministerio de Salud SALUD PUBLICA - GUIA SOBRE ANALISIS TOXICOLOGICOS Resolución (MS) 650/02. Del 30/9/2002. B.O.: 10/10/2002. Apruébase la Guía de Toma de Muestra, Conservación y Transporte para Análisis Toxicológicos, incorporándola al Programa Nacional de Garantía de Calidad de la Atención Médica. Bs. As., 30/9/2002 VISTO el Expediente Nº 1-2002-5583-02-2 del Registro del Ministerio de Salud, y CONSIDERANDO: Que las políticas tienen por objetivo primero y prioritario asegurar el acceso de todos los habitantes de la Nación a los Servicios de Salud, entendiendo por tales al conjunto de los recursos y acciones de carácter promocional, preventivo, asistencial y de rehabilitación, sean éstos de carácter público estatal, no estatal o privados; con fuerte énfasis en el primer nivel de atención. Que en el marco de las políticas del Ministerio de Salud de la Nación se desarrolla el PROGRAMA NACIONAL DE GARANTIA DE CALIDAD DE LA ATENCION MEDICA, en el cual se agrupan un conjunto de acciones destinadas a asegurar la calidad de las prestaciones en dichos Servicios. Que entre dichas acciones se encuentran la elaboración de guías de diagnóstico, tratamiento y procedimientos de patologías y normas de organización y funcionamiento de los Servicios de Salud. Que las citadas guías y normas se elaboran con la participación de Entidades Académicas, Universitarias y Científicas de profesionales asegurando de esa forma la participación de todas las áreas involucradas en el Sector Salud. Que la DIRECCION DE CALIDAD EN SERVICIOS DE SALUD, a través de su Comisión Asesora del Area de Toxicología creada por Resolución Ministerial Nº 791/97, ha coordinado el proceso de elaboración de la GUIA DE TOMA DE MUESTRA, CONSERVACION Y TRANSPORTE PARA ANALISIS TOXICOLOGICOS, de acuerdo con la normativa vigente contando con la participación del INSTITUTO NACIONAL DE ALIMENTOS (INAL-ANMAT), HOSPITAL GENERAL DE AGUDOS "DR. RICARDO GUTIERREZ", HOSPITAL GENERAL DE AGUDOS "DR. PEDRO DE ELIZALDE", HOSPITAL GENERAL DE AGUDOS "JUAN A. FERNANDEZ", HOSPITAL NACIONAL "DR. ALEJANDRO POSADAS", HOSPITAL DE PEDIATRIA S.A.M.I.C. "PROFESOR DOCTOR JUAN P. GARRAHAN", INSTITUTO ARGENTINO DE NORMALIZACION (IRAM), UNIVERSIDAD NACIONAL DE GENERAL SAN MARTIN, CENTRO DE INVESTIGACIONES TOXICOLOGICAS CEITOX (CITEFA-CONICET), CONSEJO PROFESIONAL DE QUIMICA DE LA PROVINCIA DE BUENOS AIRES, DIRECCION GENERAL DE ASESORIAS PERICIALES SUPREMA CORTE DE JUSTICIA DE LA PROVINCIA DE BUENOS AIRES, CATEDRA DE TOXICOLOGIA Y QUIMICA LEGAL DE LA FACULTAD DE FARMACIA Y BIOQUIMICA – UBA, CATEDRA DE TOXICOLOGIA Y QUIMICA LEGAL- FACULTAD DE CIENCIAS EXACTAS- UNLP, DIRECCION DE PROMOCION Y PROTECCION DE LA SALUD, PROGRAMA DE PREVENCION Y CONTROL DE INTOXICACIONES DEL MINISTERIO DE SALUD DE LA NACION, GERENCIA DE CALIDAD Y AMBIENTE-PROGRAMA DE MEDIO AMBIENTE (INTI), INSTITUTO DE BIOQUIMICA CLINICA-ROSARIO-SANTA FE Y LABORATORIO BIOTOX. Que el Comité Ejecutivo de la Asociación Internacional de Toxicólogos Forenses (TIAFT) ha autorizado la utilización de material elaborado por ese Organismo Internacional. Que la SUBSECRETARIA DE POLITICAS, REGULACION Y FISCALIZACION, COORDINADORA GENERAL DEL PROGRAMA NACIONAL DE GARANTIA DE CALIDAD DE LA ATENCION MEDICA, Y LA SECRETARIA DE POLITICAS, REGULACION Y RELACIONES SANITARIAS han tomado la intervención de su competencia y avalan su incorporación al PROGRAMA NACIONAL DE GARANTIA DE CALIDAD DE LA ATENCION MEDICA. Que la DIRECCION GENERAL DE ASUNTOS JURIDICOS ha tomado la intervención de su competencia. Que la presente medida se adopta en uso de las atribuciones contenidas por la "Ley de Ministerios T.O. 1992", modificada por Ley Nº 25.233. Por ello, EL MINISTRO DE SALUD RESUELVE: Artículo 1º — Apruébase la GUIA DE TOMA DE MUESTRA, CONSERVACION Y TRANSPORTE PARA ANALISIS TOXICOLOGICOS, que como Anexos I, II, III, IV, V y VI forman parte integrante de la presente Resolución. Art. 2º — Incorpórase la GUIA DE TOMA DE MUESTRA, CONSERVACION Y TRANSPORTE PARA ANALISIS TOXICOLOGICOS, que se aprueba en el artículo precedente al PROGRAMA NACIONAL DE GARANTIA DE CALIDAD DE LA ATENCION MEDICA. Art. 3º — Difúndase a través de la Coordinación General del Programa la citada guía, a fin de asegurar el máximo conocimiento y aplicación de la misma en el marco de dicho Programa Nacional referido en el artículo 2º precedente. Art. 4º — La guía que se aprueba por la presente Resolución podrá ser objeto de observación por las Autoridades Sanitarias Jurisdiccionales y por las Entidades Académicas, Universitarias, Científicas de Profesionales dentro del plazo de sesenta (60) días a partir de la fecha de su publicación en el Boletín Oficial y en caso de no ser observada entrará en vigencia a los noventa (90) días de dicha publicación. Art. 5º — En el caso que la autoridad jurisdiccional realizara alguna adecuación a la presente norma para su aplicación a nivel de la jurisdicción deberá comunicar a la COORDINACION GENERAL DEL PROGRAMA dicha adecuación, la que recién entrará en vigencia a los sesenta (60) días de su registro a nivel nacional a través del acto administrativo correspondiente. Art. 6º — Agradecer a las entidades participantes, INSTITUTO NACIONAL DE ALIMENTOS (INALANMAT), HOSPITAL GENERAL DE AGUDOS "DR. RICARDO GUTIERREZ", HOSPITAL GENERAL DE AGUDOS "DR. PEDRO DE ELIZALDE", HOSPITAL GENERAL DE AGUDOS "JUAN A. FERNANDEZ", HOSPITAL NACIONAL "DR. ALEJANDRO POSADAS", HOSPITAL NACIONAL DE PEDIATRIA "DR. PEDRO GARRAHAN", INSTITUTO ARGENTINO DE NORMALIZACION (IRAM), UNIVERSIDAD NACIONAL DE GENERAL SAN MARTIN, CENTRO DE INVESTIGACIONES TOXICOLOGICAS (CEITOX- CITEFA), CONSEJO PROFESIONAL DE QUIMICA DE LA PROVINCIA DE BUENOS AIRES, DIRECCION GENERAL DE ASESORIAS PERICIALES SUPREMA CORTE DE JUSTICIA DE LA PROVINCIA DE BUENOS AIRES, CATEDRA DE TOXICOLOGIA Y QUIMICA LEGAL DE LA FACULTAD DE FARMACIA Y BIOQUIMICA – UBA, CATEDRA DE TOXICOLOGIA Y QUIMICA LEGAL- FACULTAD DE CIENCIAS EXACTAS- UNLP, DIRECCION DE PROMOCION Y PROTECCION DE LA SALUD, PROGRAMA NACIONAL DE PREVENCION Y CONTROL DE INTOXICACIONES DEL MINISTERIO DE SALUD DE LA NACION, GERENCIA DE CALIDAD Y AMBIENTE-PROGRAMA DE MEDIO AMBIENTE(INTI), INSTITUTO DE BIOQUIMICA CLINICA-ROSARIO-SANTA FE y LABORATORIO BIOTOX por la importante colaboración brindada a este Ministerio. Art. 7º — De forma. GUIA PARA LA OBTENCION DE MUESTRA, CONSERVACION, TRANSPORTE Y ANALISIS TOXICOLOGICOS
INDICE:
ANEXO I. Introducción ANEXO II. Obtención de muestra y cadena de custodia ANEXO III. Guía para la obtención, transporte, conservación y análisis de muestras en pacientes con probable intoxicación aguda ANEXO IV. Guía para la obtención, transporte, conservación y análisis de muestras en pacientes con probable intoxicación crónica ANEXO V. Guía para la obtención, transporte, conservación y análisis de muestras en pacientes con probable intoxicación por alimentos ANEXO VI. Laboratorios de Análisis Toxicológicos de la República Argentina
INTRODUCCION El análisis toxicológico aplicado a la clínica, la pericia forense, el análisis de alimentos o destinado a la evaluación de un riesgo asociado a la exposición humana a las sustancias químicas, constituye una parte relevante de la práctica profesional. A través del tiempo, el análisis toxicológico ha ido evolucionando desde primitivas estrategias de identificación, orientadas por grupos de sustancias, mediante metodologías sencillas, hasta las disponibles hoy por medio de instrumental de alta complejidad. Frente a la demanda de análisis toxicológicos, de por sí variados y técnicamente complejos, resulta imprescindible que el laboratorio cuente con una capacidad de respuesta apropiada. Para ello el proceso analítico deberá cumplir con un elevado criterio de calidad, considerando disponibilidad, confiabilidad, especificidad y sensibilidad del método elegido. La obtención de la muestra constituye el primer eslabón de ese proceso y es el que condicionará las etapas siguientes del análisis hasta llegar al resultado, por lo que establecer pautas claras en esta etapa crítica no resulta ocioso. Nuestro país carece hoy de una norma al respecto y los laboratorios aplican protocolos de diversas procedencias o bien se sigue un criterio personal siguiendo los principios de la Química Analítica. El propósito de esta publicación es servir de guía u orientación al profesional que actúa en las distintas etapas del análisis toxicológico, conteniendo recomendaciones racionales y sencillas, adaptadas lo mejor posible a los medios disponibles en nuestro país. En el presente documento se plantean distintos aspectos del análisis toxicológico, desde los estrictamente técnicos como criterios sobre selección, preparación y conservación de las muestras, hasta los aspectos legales asociados a los análisis como cadena de custodia y confidencialidad de los resultados. Se han agregado también recomendaciones sobre la forma óptima de funcionamiento de un laboratorio que vaya a realizar este tipo actividad. PROCEDIMIENTOS DE LABORATORIO PARA EL ANALISIS TOXICOLOGICO Los análisis toxicológicos involucran la detección, la identificación y la cuantificación de las sustancias con relevancia toxicológica y la interpretación de los resultados. Con el propósito de que estos últimos sean confiables deben aplicarse estándares de calidad. Las recomendaciones que siguen pretenden servir como una base sobre la cual puedan desarrollarse prácticas y metodologías adecuadas y se aplican al análisis de principios activos o metabolitos de fármacos, drogas de abuso y toda otra sustancia con relevancia toxicológica (ej. alcohol, metales, pesticidas, etc.) en el sentido más amplio, presentes principalmente en muestras biológicas, fluidos corporales humanos, tejidos, etc. Esto incluye: a) Detección de tóxicos y su relevancia en la determinación de la causa de intoxicación y/o muerte. b) Análisis de fármacos y/o de drogas de abuso que puedan afectar el comportamiento humano. c) Análisis cuali y/o cuantitativo de drogas en material biológico, humano y animal, u otros especímenes (alimentos, medicamentos y compuestos usados en medicina popular). d) Mal uso de sustancias en relación con las actividades deportivas (dopaje). Además de los análisis cualitativos y cuantitativos como tales, debe considerarse a la interpretación de los resultados analíticos como una parte integral del análisis toxicológico. 1. Laboratorio y el personal 1.1. Laboratorio El laboratorio para el análisis toxicológico debe contar con la habilitación o autorización para funcionar emanada de la autoridad sanitaria correspondiente. Sus instalaciones deben cumplir con un estándar científico aceptable. Tanto éstas como los procedimientos que se lleven a cabo deben permitir un manejo seguro de las muestras potencialmente infecciosas y/o tóxicas, y prohibir el acceso a los especímenes a las personas no autorizadas. Los procedimientos de laboratorio deben asegurar la detección, la identificación y la cuantificación de sustancias individuales (no de grupos). Actualmente, las técnicas que se consideran aceptables aceptables incluyen la TLC (cromatografía en capa delgada), GC (cromatografía de gases), HPLC (cromatografía líquida de alta performance), MS (espectrometría de masas), métodos espectroscópicos (ej. UV/VIS, IR y absorción atómica) y el inmunoanálisis (ej. RIA, EMIT, FPIA, etc.). Las limitaciones en la disponibilidad de metodologías no necesariamente deben disminuir la confiabilidad de los resultados, siempre y cuando cualquier debilidad sea aclarada en el informe, aunque evidentemente limitará el alcance y la excelencia del proceso analítico (respecto a los analitos detectables, a los límites de detección, al significado de los procedimientos de cuantificación, el número de muestras que se puedan procesar, etc.). 1.2. Personal El laboratorio toxicológico debe ser dirigido por un profesional con título universitario habilitante en Ciencias Bioquímicas o Químicas, otorgado por autoridad competente, y con probados entrenamiento y experiencia en Toxicología Analítica. Cualquier miembro del cuerpo técnico del laboratorio debe tener una educación profesional adecuada a las responsabilidades particulares dentro del equipo. El director debe: 1) Asegurar que el personal del laboratorio está entrenado adecuadamente y tiene experiencia suficiente para llevar a cabo el trabajo del laboratorio y, 2) Mantener la competitividad del personal del laboratorio a través del monitoreo de la calidad de su trabajo y verificando su pericia, incluyendo su capacidad para actuar como testigo experto para los propósitos de presentar evidencia. 2. Muestras y su recepción La selección apropiada, la recolección y la remisión de muestras biológicas y de otro tipo para el análisis toxicológico son de importancia fundamental para la producción de resultados significativos y precisos, así como también para la interpretación subsecuente de los mismos. El director del laboratorio debe desarrollar y proveer guías e instrucciones precisas a todas las partes que les remitan muestras. Estas instrucciones deben establecer las cantidades mínimas necesarias de cada tipo de espécimen para llevar a cabo los análisis y las subsecuentes interpretaciones. Siempre que sea posible, la cantidad de muestra recolectada debe ser suficiente para asegurar la existencia de un remanente para efectuar un re-análisis, si así fuese solicitado. Las instrucciones deben incluir requerimientos específicos para el tipo y el tamaño de los contenedores, y si correspondiera, el tipo y cantidad de preservante que se agregará a los fluidos biológicos. Las instrucciones para el rotulado de los contenedores individuales, las condiciones aceptables para el embalaje y el transporte también deben quedar bien establecidas. Los remitentes deben ser instruidos sobre cómo identificar claramente (con palabras como "infeccioso", explicado en los formularios adjuntos) todos los especímenes de sujetos vivos o fallecidos que pudieran portar alguna enfermedad muy infecciosa tal como hepatitis, tuberculosis o el virus de la inmunodeficiencia humana (HIV). Los especímenes recibidos en el laboratorio deben identificarse adecuadamente y almacenarse de un modo seguro, a una temperatura apropiada, protegidos de la luz de manera tal que se asegure la salvaguarda de su integridad. Donde sea necesario deben seguirse procedimientos aceptables de cadena de custodia cuando los especímenes se transfieren de un lugar a otro y especialmente en aquellos centros que procesen grandes volúmenes de muestras. Los procedimientos deben minimizar cualquier posibilidad de error en la identificación o de contaminación. Luego del análisis inicial, debe guardarse un resto o un duplicado del espécimen en condiciones apropiadas por un lapso determinado (dependiendo de los analitos, del tipo de espécimen y del propósito del análisis) de modo que permita un re-análisis, si fuese necesario. Este tiempo debe contemplar el proceso legal involucrado y cualquier regulación que establezca un período mínimo de almacenamiento (ver Anexos). 3. Trabajo técnico en el laboratorio 3.1. Aseguramiento de la identidad de la muestra Todas las alícuotas y extractos deben rotularse adecuadamente para asegurar la integridad de los resultados analíticos. Donde sea necesario, el paso del espécimen por el laboratorio debe documentarse en un formulario de cadena de custodia. 3.2 Métodos Deben existir instrucciones claras y escritas para todos los métodos y procedimientos utilizados en el laboratorio (manual de procedimientos estándar). Los métodos deben contener información suficiente, de modo tal que el personal calificado pueda seguir los procedimientos luego de un período breve de instrucción. Los métodos y procedimientos deben validarse apropiadamente. Todos los procedimientos tienen que ser aprobados por el director del laboratorio toxicológico. Cualquier modificación en el método o procedimiento debe documentarse claramente, estableciendo las razones para esos cambios. Por último, todos los cambios deben ser aprobados por el director del laboratorio u otro personal jerárquico autorizado. 3.3 Análisis 3.3.1. Detección En el análisis cualitativo, el objetivo principal es detectar las sustancias de relevancia toxicológica. Dependiendo de la razón del análisis, deberán seguirse distintas estrategias analíticas. Si el análisis toxicológico tiene como propósito el detectar un solo tóxico, o un grupo de tóxicos, podrán aplicarse procedimientos específicos (análisis toxicológico dirigido). Siempre que sea posible, deben aplicarse al menos dos procedimientos diferentes, cada uno de éstos utilizando un principio físico o químico distinto, para permitir la detección y confirmación de la sustancia sin ambigüedad. Si el análisis se realiza para detectar o para excluir un rango amplio de tóxicos sin una dirección específica ("desconocido general"), el procedimiento adecuado será la estrategia analítica compleja del Análisis Toxicológico Sistemático. Su finalidad es detectar todas las sustancias de relevancia toxicológica, y en casos positivos identificarlas inequívocamente por exclusión de todas las demás. Para este fin deberán correrse en paralelo o en secuencia, una serie de procedimientos basados en una variedad de principios analíticos. Debe notarse que este principio requiere usualmente que el ensayo de "screening" sea seguido por uno de confirmación. Con el propósito de caracterizar el grado de certidumbre de la identificación, en el informe deben establecerse aquellos métodos que se utilizaron para llegar a las conclusiones reportadas. Si no pudiera llevarse a cabo un ensayo confirmatorio independiente (ej. si hay disponible un solo procedimiento analítico, o no hay cantidad suficiente de muestra), ésto debe ser declarado en el informe, ya que disminuye la certidumbre de la identificación. 3.3.2. Cuantificación Normalmente el análisis cuantitativo deberá aplicarse cuando se espere una interpretación basada en los niveles del analito. La cuantificación se realizará sobre una alícuota de la muestra, distinta a la utilizada para la búsqueda y/o el análisis cualitativo. 3.3.2.1. Calibración Siempre que sea posible, deben emplearse procedimientos de estándar interno, puesto que esto minimiza los errores debidos a la adsorción en superficies, a la pérdida durante la extracción, a las pérdidas durante la evaporación del solvente, o durante los procedimientos de derivatización, y la irreproducibilidad debida a las técnicas de transferencia y de inyección. Los estándares internos deben ser, idealmente, un homólogo del analito. Si esto no es posible, se elegirá un compuesto que posea propiedades físico-químicas similares a las del analito. Las propiedades cromatográficas del estándar interno deben ser tales que eluya muy cerca del analito pero aún así, completamente resuelto de cualquier otra sustancia presente. Cuando sea posible, el estándar interno debe prepararse en solución acuosa y mezclado con la muestra previamente al análisis. Las curvas de calibración deben prepararse a partir de estándares en el mismo tipo de matriz que tiene la muestra, y los estándares deben analizarse utilizando el mismo procedimiento de extracción aplicado al analito. La curva de calibración debe construirse desde la relación entre la respuesta del detector y la concentración del analito, usando los procedimientos para estándar interno. Si no se prepara una curva de calibración completa, los estándares cuantitativos deben comprender el rango de concentración del analito presente. Los resultados deben expresarse sin ambigüedad y deben utilizarse preferentemente unidades de concentración del Sistema Internacional. 3.3.2.2. Validación Todos los métodos deben validarse utilizando la misma matriz primaria que será común en el análisis (ej. sangre, suero, tejido). A esas matrices se agregarán cantidades conocidas de las sustancias y se llevará a cabo el procedimiento analítico completo. De todos modos, el criterio para esta validación también dependerá del propósito del análisis. Esto puede significar que un límite de detección muy bajo podría no ser relevante para una investigación determinada. Aquellos criterios a validarse son: Exactitud, precisión, recuperación absoluta (ensayada a diferentes concentraciones), rango de calibración, selectividad, límite de cuantificación y posible robustez del método. También se evaluarán el tiempo y el costo del análisis. Los reactivos deben ensayarse por procedimientos de aseguramiento de la calidad. Deben realizarse análisis por duplicado siempre que sea posible. Los métodos cromatográficos de cuantificación siempre deben preferirse a otros más clásicos (ej. al uso directo de la espectroscopía UV), puesto que la cromatografía puede separar la droga de sus metabolitos y de otras sustancias interferentes. El rango de concentraciones para el cual el método es válido debe ser lo suficientemente grande para incluir todas las concentraciones que son factibles de encontrarse en la realidad (ej. terapéutica, tóxica y fatal). 4. Revisión y documentación de los resultados 4.1. Aseguramiento de la calidad (AC) y control de la calidad (CC) Se recomienda que los laboratorios tengan su propio programa interno de control de la calidad y de aseguramiento de la calidad, pero que también participen en programas de ensayo de aseguramiento de calidad y de capacidad, siempre que sea posible. Dependiendo del tipo de análisis (desconocidos generales, análisis cualitativos especiales, cuantificaciones), se hace necesario un control de calidad orientado por método o por sustancia. 4.2. Documentación de los resultados Los resultados de todos los análisis deben documentarse en su totalidad. Este registro escrito debe incluir toda la información necesaria para identificar el caso y su fuente (junto con toda la información adicional acerca de las circunstancias características del caso), una lista de los especímenes analizados, las sustancias o grupos de sustancias investigadas, deben contener todos los resultados de los ensayos y los métodos utilizados (explícitos o codificados), y deben llevar la firma del individuo que tiene la responsabilidad de su contenido. Esta información debe ser fácilmente recuperable. 4.3. Revisión de los resultados Antes que los resultados se informen, cada grupo de datos analíticos debe ser revisado por el personal científico que tiene experiencia en los protocolos analíticos usados en el laboratorio. Como mínimo, esta revisión incluirá: documentación de cadena de custodia, validez de los datos analíticos (ej. forma y relación señal-ruido en los picos cromatográficos), cálculos y cualquier otro dato de control de calidad. La revisión debe documentarse dentro del registro analítico. 5. Informe Se preparará un informe escrito para la parte que requirió el análisis. La extensión de este informe depende de lo solicitado. Por ejemplo, un informe para un tribunal judicial posiblemente necesite ser más extenso que uno cuyo fin es reportar un resultado negativo en un ensayo de monitoreo de drogas de abuso. El informe debe contener el tipo de muestras analizadas y los analitos (sustancias o grupos de sustancias) investigados. Los métodos utilizados para los ensayos normalmente serán establecidos por tipo e incluirán algún párrafo aclaratorio si los resultados son menos confiables que lo normal (por ejemplo, si no se incluyó algún método identificatorio de alta confiabilidad o si algún ensayo confirmatorio no se pudo llevar a cabo por las razones descritas en 3.3.1.) Los resultados finales tienen que estar establecidos claramente y caracterizados por el correspondiente grado de certeza. El informe se terminará con la interpretación del significado de los resultados para el propósito del análisis. Debido a que los resultados son confidenciales, deberán tomarse todas las precauciones para asegurar que solamente la persona autorizada reciba la información (especialmente cuando ésta se transmite por fax, computadora o teléfono). Cada laboratorio debe formular su propia regulación para la retención y liberación de la información. Toma y remisión de muestras en el análisis toxicológico clínico, laboral y forense. La adecuada selección, recolección, preservación y envío de especímenes biológicos y cualquier otra muestra con el propósito de un estudio toxicológico es de fundamental importancia. El éxito de un análisis y su interpretación depende en grado sumo de esta etapa. Si bien no todo estudio analítico toxicológico puede terminar en el ámbito judicial, los acontecimientos extraordinarios acaecidos en las dos últimas décadas nos han enseñado a movernos con prudencia en este sentido. En el Anexo II se describen los procedimientos de toma de muestra y de cadena de custodia.
TOMA DE MUESTRA Y CADENA DE CUSTODIA l. Materiales biológicos que deberían remitirse al laboratorio clínico toxicológico Tipos de muestras a considerar: sangre o suero, orina, vómito, contenido o lavado gástrico, pelos, uñas, saliva. I.2. Modo correcto de remitir el material para estudio A. Sangre Para la toma de muestra se desinfectará la piel con alcohol, excepto en el caso de determinación de alcoholemia (en este caso recurrir a solución jabonosa, agua oxigenada, iodopovidona, etc.). Ante la sospecha de una intoxicación de origen desconocido se deberá recoger la muestra de sangre en dos tubos, uno de ellos con anticoagulante (preferentemente heparina) y otro tubo sin anticoagulante (o con gel acelerador de coagulación). En el caso de tener que asegurar la estabilidad de la muestra, se recomienda reemplazar la heparina por fluoruro de sodio al 1% (como preservador antibacteriano). El volumen recomendable en cada caso será de 5 ml. La conservación de la muestra se hará en heladera a 4°C. Los recipientes que se envían deben ser tubos de polipropileno o similar con cierre hermético. Es preferible utilizar material nuevo o virgen, para evitar contaminaciones (muchas veces quedan restos de medicamentos u otras sustancias que no se extraen con lavado "casero", provocando confusiones en el ulterior estudio analítico). Cuando se envasa sangre o suero, NO DEBE QUEDAR ESPACIO VACIO EN EL RECIPIENTE, es decir se debe evitar la formación de una cámara de aire, que produce pérdidas importantes no sólo de etanol sino de cualquier otro tóxico volátil. Para evitar ésto , el recipiente debe ser llenado al ras, bien tapado y si es posible sellado. Los recipientes que serán utilizados para colocar sangre o suero NO DEBEN ENJUAGARSE NUNCA CON ALCOHOL. Para determinados tóxicos podrán variarse el tipo de anticoagulante, el volumen de la muestra y su conservación (ver anexo). En los casos de extracciones a imputados de un ilícito, se recomienda la extracción de por lo menos DOS muestras sanguíneas consecutivas, con intervalo de una hora entre ambas extracciones. Cada muestra se rotulará claramente y se anotará la hora a la que fueron extraídas (importante para determinación de alcoholemias retrospectivas). B. Orina Este tipo de muestra es idónea para realizar un estudio de "screening" en el caso de no conocer el origen de la intoxicación. Otra ventaja es que la concentración del analito puede ser mayor que en sangre. Además, en general, la orina está exenta de proteínas, con lo cual se tienen menos interferencias. Es una muestra más abundante, fácil de recolectar y de conservar. Procedimiento para su recolección: Emplear un recipiente limpio. En algunos casos es conveniente recolectar el volumen total de 24 horas y en otros resultan útiles las orinas ocasionales, según se describe en el Anexo. Por lo general es conveniente conservarla en la heladera, a 4 °C o bien el freezer (ver anexo para mayores detalles). Il. Materiales biológicos que deberían remitirse al laboratorio toxicológico forense Tipos de muestras en el caso de individuos fallecidos: Sangre, orina, vísceras: pulmón, corazón, cerebro, tráquea, hígado, riñón, bazo, tejido adiposo (grasa), pelo (pericraneal, púbico, axilar), uñas, humor vítreo, bilis. II.1. Modo correcto de remitir el material para estudio A. Vísceras Deben colocarse en recipientes rigurosamente limpios, sin agregado de ningún tipo de sustancia con fines de preservación u otro motivo. Debe disponerse de un recipiente para cada órgano. Como mínimo se deben obtener muestras de los siguientes órganos: hígado, estómago y su contenido, cerebro, pulmón y riñón. En casos particulares, a criterio del profesional interviniente, se podrán agregar muestras de otros órganos. Los fluidos biológicos también deberán estar en recipientes individuales. Los recipientes pueden ser de vidrio incoloro, aunque si se dispone de frascos de vidrio color caramelo, estos serán apropiados especialmente para sustancias que se conozcan como fotosensibles. El tamaño debe estar en relación con el de la muestra, evitando en lo posible la existencia de cámaras de aire. El cierre debe ser perfecto. Si no es posible, sellar con parafina. No deben usarse tapas de papel, algodón ó cartón. Pueden utilizarse recipientes plásticos con tapas del mismo material que permitan un cierre perfecto. Actualmente hay disponibles bolsas plásticas de distintos tamaños para envasar las muestras, con un tipo de cierre inviolable; es decir, si se pretende abrir los recipientes una vez cerrados, se destruye el material, pudiéndose detectar así maniobras dolosas de apertura. Las muestras deben rotularse correctamente, con datos apropiados mínimos y legibles, que correspondan al hecho (identificación de la víctima, juzgado interviniente, fecha y número de causa), que no den lugar a confusión, utilizando marcadores de tinta indeleble. La conservación de las muestras hasta su análisis será a una temperatura ideal de (–20°C), a la cual la actividad enzimática en los sistemas biológicos se halla prácticamente paralizada. Estudios de degradación de analitos muestran que a estatemperatura los tejidos y humores biológicos sufren poca pérdida de los mismos por biotransformación. Se admitirá la conservación a 4°C siempre que el tiempo no supere las 24 horas. En el caso de sospecha de tóxicos volátiles sólo se admitirá la conservación a (–20°C). Las muestras serán embaladas en recipientes apropiados para conservar el frío, asegurando que los recipientes contenidos dentro de la caja de transporte no puedan sufrir roturas durante el traslado al laboratorio. Es importante respetar el mantenimiento de la cadena de frío durante el traslado, manteniendo las condiciones iniciales de temperatura. B. Sangre Es necesario como mínimo 10 ml de muestra para someter este fluido a estudio toxicológico general. En el caso de análisis de alcoholemia se requieren 2 ml. Los recipientes utilizados para recoger las muestras deben ser tubos de polipropileno o similar con cierre hermético. Es conveniente utilizar material nuevo o virgen, para evitar contaminaciones. Agregar fluoruro de sodio al 1% como preservador. NO ENJUAGAR NUNCA CON ALCOHOL los recipientes que serán utilizados para recoger sangre o suero ni tampoco dejar un ESPACIO VACIO EN EL RECIPIENTE, es decir, se debe evitar la formación de una CAMARA DE AIRE que produce pérdidas importantes no sólo de etanol sino de cualquier tóxico volátil. Si bien aún hay discrepancias entre los investigadores acerca de cuál es la zona donde se minimizan las variaciones en la concentración de los analitos, la vena femoral o la cavidad intracardíaca son las más utilizadas. La conservación de las muestras de sangre debe hacerse a 4°C. C. Orina Muestra postmortem: Remitir toda la muestra existente en vejiga, en forma similar a la recolección sanguínea, colocada en recipientes de mayor capacidad. Rotular y cerrar perfectamente. Anotar día, mes y hora de emisión o recolección y fecha y hora de una dada circunstancia por la que se le pide la determinación.(v.g: determinación de cocaína o metabolitos). NO AGREGAR NINGUNA SUSTANCIA COMO CONSERVANTE. Refrigerar a 4°C. D. Pelo Forma de recolección: Cortar en el sector occipital, bien al ras del cuero cabelludo,1 ó 2 gramos de muestra (en la práctica un puñado o mechón es suficiente). Tomar el extremo cercano al cuero cabelludo, colocarlo sobre papel o cartón y abrochar con aplique de broches de tamaño apropiado, colocar otro papel o cartón encima del anterior y pegar o atar según corresponda. El envoltorio debe permanecer firme. Indíquese claramente la zona cercana al cuero cabelludo y la distal. Tomar vello pubiano y axilar, cortado al ras de la piel y colocarlo en sobre de papel común. E. Humor vítreo Se realiza resecando completamente el globo ocular o bien a través de una punción del mismo con aguja y jeringa; muchas veces se remite humor acuoso y no humor vítreo ya que la densidad de éste último hace dificultosa la extracción; por lo tanto debe ponerse atención cuando se envía esta matriz. F. Diferentes líquidos corporales La obtención se debe realizar por punción de las cavidades donde estos se encuentran cuidando de no contaminar un líquido con otro ( líquido ascítico, de derrame pleural, pericárdico, líquido amniótico, etc). Las secreciones más viscosas pueden obtenerse con pipetas o hisopos de algodón (existen en el mercado pipetas descartables de material plástico y bajo costo con sistema aspirativo, sin necesidad de trasvasar el contenido). CADENA DE CUSTODIA En el análisis toxicológico es de suma importancia asegurar la identificación, la certeza y la integridad de una muestra que se remite al laboratorio. Durante el proceso de recolección, algunos individuos tratan de falsificar el espécimen mediante el agregado de diferentes sustancias como por ejemplo: sales, solventes, sustancias enmascarantes, o bien reemplazan una muestra por otra. Esta delicada situación se presenta especialmente con las muestras de orina, por lo que se deben tomar ciertos recaudos que eviten la adulteración de la misma. Ellos incluyen: - Verificación de la identidad del donante - Vigilancia directa del donante durante la emisión de la orina - Evaluación del aspecto y de la temperatura de la muestra - Medición del pH y de la densidad: permite considerar si se alcalinizó o diluyó la muestra El control del muestreo y de todas las etapas subsiguientes que forman parte del análisis toxicológico deben contar con una cadena de custodia que permita asegurar que la muestra analizada es, en todo momento del proceso analítico y aún terminado éste*, la misma que fue recogida. La cadena de custodia es " el procedimiento que asegura que la muestra que se procesa en el laboratorio toxicológico no sea alterada, sustituida, cambiada o manipulada entre el momento en que ésta se recoge hasta el momento que finaliza el análisis". Para cumplir con el objetivo es conveniente que el laboratorio cuente con una normativa escrita para la aplicación de cada paso de la cadena de custodia y que la misma sea conocida por quienes intervienen en ella. Dado que desde el inicio hasta el final del entero proceso la muestra puede ser manipulada por varias personas, la participación de las mismas debe quedar debidamente documentada, de manera tal que si hay una intervención judicial no se desplome la evidencia. —————————— *Reserva de material para contraprueba.
CADENA DE CUSTODIA GUIA PARA EL TRANSPORTE DE MUESTRAS BIOLOGICAS PARA ANALISIS TOXICOLOGICOS Los objetivos de estas guías son: - Preservar la integridad de la muestra - Contemplar los factores que puedan afectarla, poniendo en riesgo la certeza del resultado - Garantizar el cumplimiento de las condiciones de bioseguridad para el traslado de este tipo de material Acondicionamiento de las muestras para el transporte: Deberán respetarse las siguientes condiciones: 1- Recipiente primario: es el que contiene el material a transportar. Puede ser de polipropileno o poliestireno cerrado herméticamente a fin de evitar pérdidas. En el caso de ser de vidrio deberán tomarse todos los recaudos que prevengan la rotura. Todos los componentes del contenedor que estén en contacto con la muestra deberán estar libres de sustancias que puedan interferir con el test de laboratorio y su resultado. 2- Recipiente secundario: es el que contiene el o los recipientes primarios. Debe ser de un material irrompible, con tapa con cierre hermético y de volumen adecuado que permita retirar el recipiente primario. Debe contener un material absorbente: papel, algodón o paño capaz de absorber el fluido contenido en el recipiente primario en el caso de que éste se dañe. Varios recipientes primarios pueden disponerse en recipientes secundarios. En este caso se deberá cumplir: a- Que el volumen total de los recipientes primarios no exceda los 50 ml. b- Establecer un sistema de separación de los recipientes primarios de manera de impedir choque entre ellos. c- Disponer los recipientes primarios de manera tal que se permita colocar material absorbente capaz de absorber fluidos contenidos en los recipientes primarios. d- En el exterior del recipiente secundario se deberá colocar la información que se detalla en rótulos. Temperatura de envío de las muestras: La muestra deberá transportarse refrigerada entre 4 y 8°C. Para ello se utilizará un recipiente terciario que corresponde al recipiente de transporte exterior. Debe ser de un material que resista el peso y el daño relacionado con la manipulación, el embarque y transporte. Consideraciones especiales para el transportre de muestra en cadena de frío: Los transportes respetando la cadena de frío, requieren de acondicionamiento especial con material, apto para mantener la temperatura, usualmente el utilizado es el llamado hielo seco o dióxido de carbono. Los contenedores terciarios de poliestireno de grosor adecuado son los apropiados pues permiten la liberación del gas de dióxido de carbono y evitan la concentración de presión que podría romper el paquete. El hielo seco debe ser colocado entre el recipiente secundario y el terciario. La cantidad depende de la capacidad de aislamiento del contenedor de traslado y del tiempo que la muestra recorrerá en su traslado. El exceso de espacio aéreo o de material de envoltura, dentro del contenedor de traslado puede causar que el hielo seco se disipe rápidamente. Etiquetado y rotulación: Todos los rótulos y etiquetas deben efectuarse con elementos de escritura indelebles para evitar que se borren por efecto de la humedad o rotura de los contenidos. Todos los datos de identificación del material deben constar en el envase secundario. La información que debe contener la ficha es la siguiente: • Descripción del material • Responsable: Institución en la cual se obtuvo la muestra. Dirección completa • Lugar de destino (describir Instituciones y Responsables) • Cantidad de material en el interior • Fecha de salida • Plan de contingencia • Cadena de frío Plan de Contingencia Todo material que sea transportado deberá ser acompañado de un informe sobre la conducta a seguir en caso de pérdida y/o roturas del contenido. Estas indicaciones deberán en forma clara, describir las acciones de manipuleo para destruir, inactivar en forma química o física el material, de así requerirse para proceder a su destrucción. Las indicaciones deben por lo tanto advertir de los requerimientos para que terceros puedan efectuar las tareas en condiciones de seguridad. Cualquier eventualidad deberá notificarse a la autoridad sanitaria competente quien podrá además determinar medidas complementarias como desinfección, aislamiento e inmunoprofilaxis activa y pasiva, si así correspondiera. —————————— Para la confección de esta guía se ha tomado como referencia la resolución Nº 54/1998 del Ministerio de Salud de la Nación.
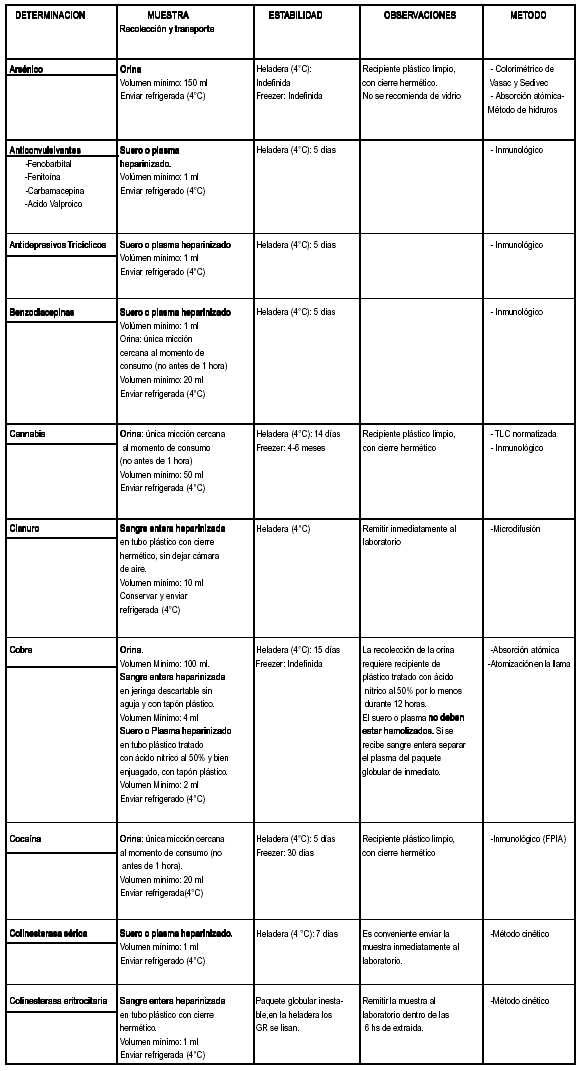
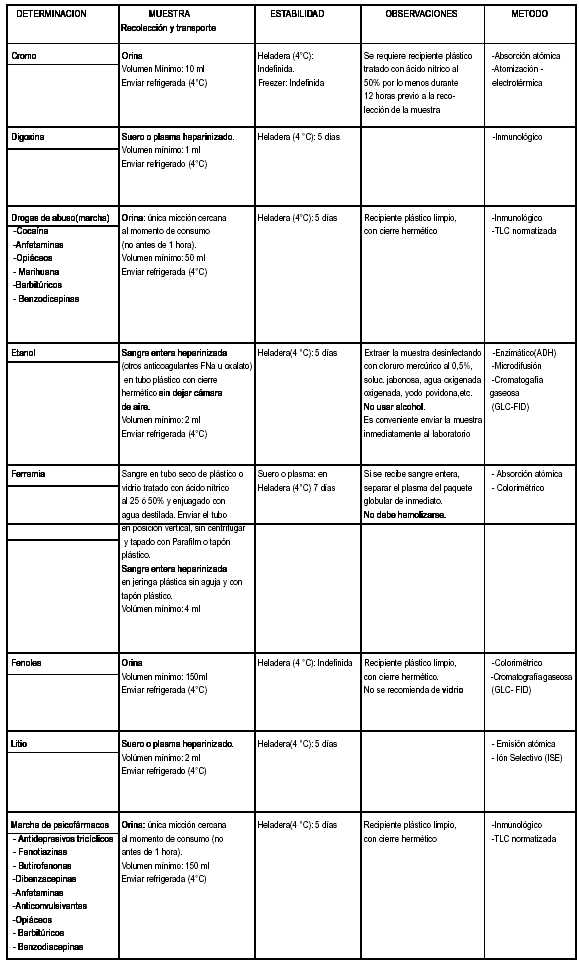
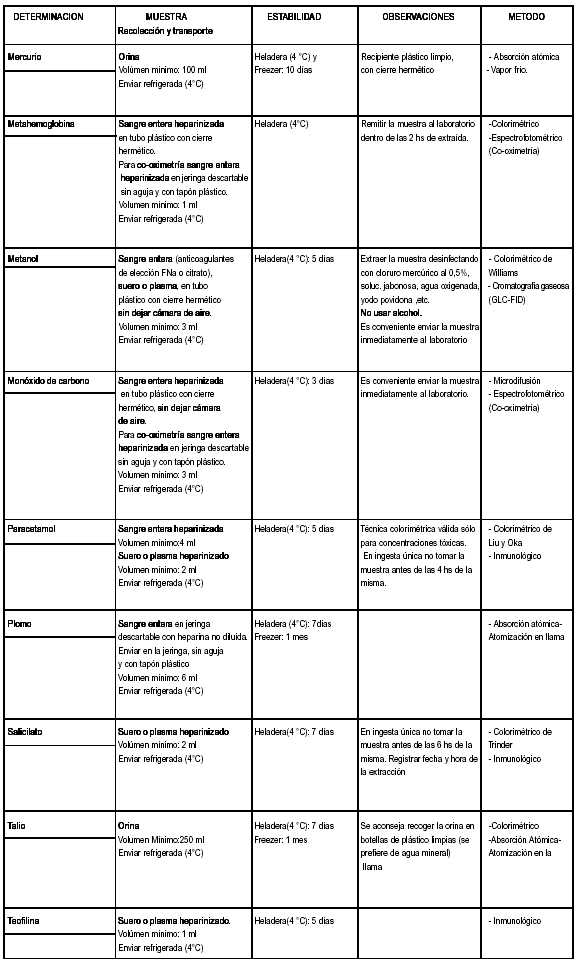
GUIA PARA LA OBTENCION, TRANSPORTE, CONSERVACION Y ANALISIS DE MUESTRAS EN PACIENTES CON PROBABLE INTOXICACION AGUDA INTOXICACIONES AGUDAS REMISION DE MUESTRAS AL LABORATORIO La obtención del material biológico es una etapa fundamental del análisis toxicológico que permite obtener resultados análiticos confiables. Los datos que brinda el laboratorio, en conjunto con la clínica del paciente, ayudarán al médico al diagnóstico certero de las intoxicaciones. La recolección, el transporte y el almacenamiento de las muestras debe hacerse de manera tal que permitan asegurar la conservación del analito y evitar la alteración y contaminación del material remitido. Las muestras deberán colocarse en recipientes limpios, secos, libres de todo contaminante y con cierre hermético para evitar derrames durante el transporte. Con respecto al tiempo de recolección se tendrá en cuenta el tiempo trasnscurrido desde el momento de contacto, la vida media del analito, el estado clínico del paciente y la urgencia del caso. Cuando se sospecha una intoxicación aguda, se recomienda recolectar una muestra de orina dentro de las 24 hs del ingreso del paciente a la Unidad Hospitalaria y conservarla en condiciones adecuadas hasta el momento que el médico decida descartar o confirmar la probable intoxicación. Las muestras deberán mantenerse a 4 °C y enviarse al laboratorio lo antes posible. El correcto almacenamiento del material biológico impide la alteración por procesos de putrefacción y la descomposición de los tóxicos por acción de la temperatura, de la luz o procesos de oxidación o hidrólisis. Las muestras deberán estar claramente identificadas y acompañadas por los protocolos de envío de muestras y cadena de custodia debidamente completadas. Consultar con los Laboratorios Toxicológicos de referencia ante cualquier duda en la interpretación de esta Guía o casos particulares que no hayan sido contemplados. GUIA PARA OBTENCION,TRANSPORTE Y CONSERVACION DE MUESTRAS EN PACIENTES CON PROBABLE INTOXICACION AGUDA
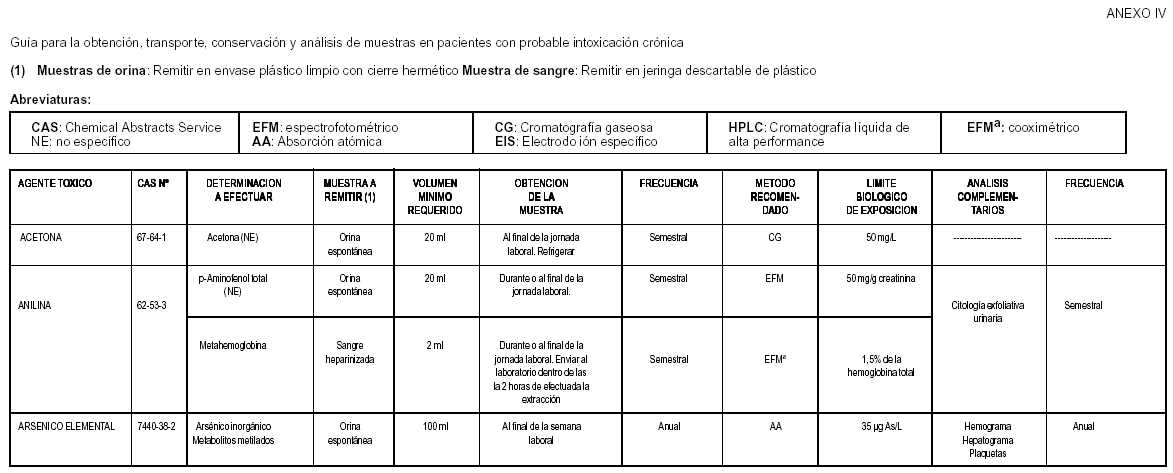
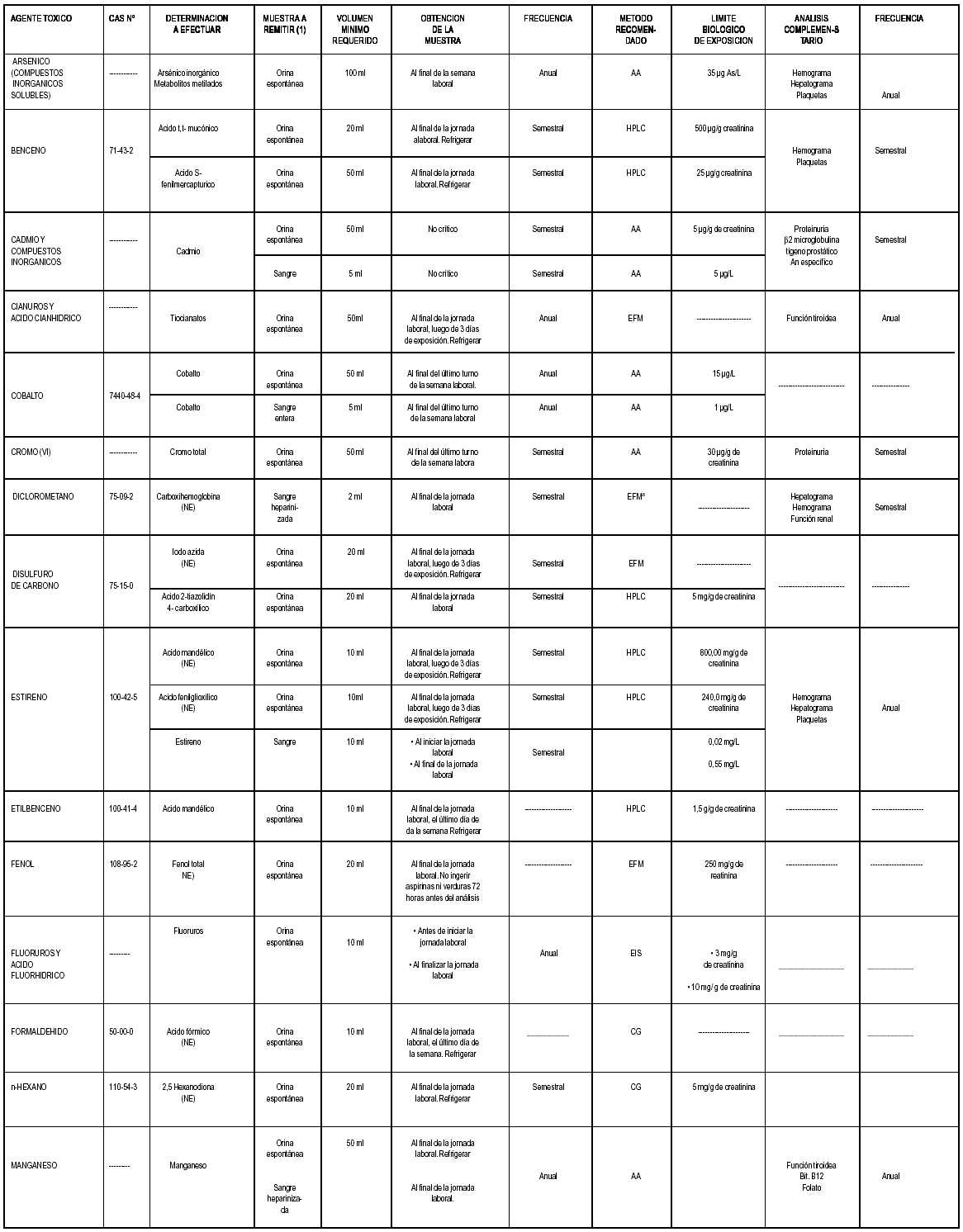
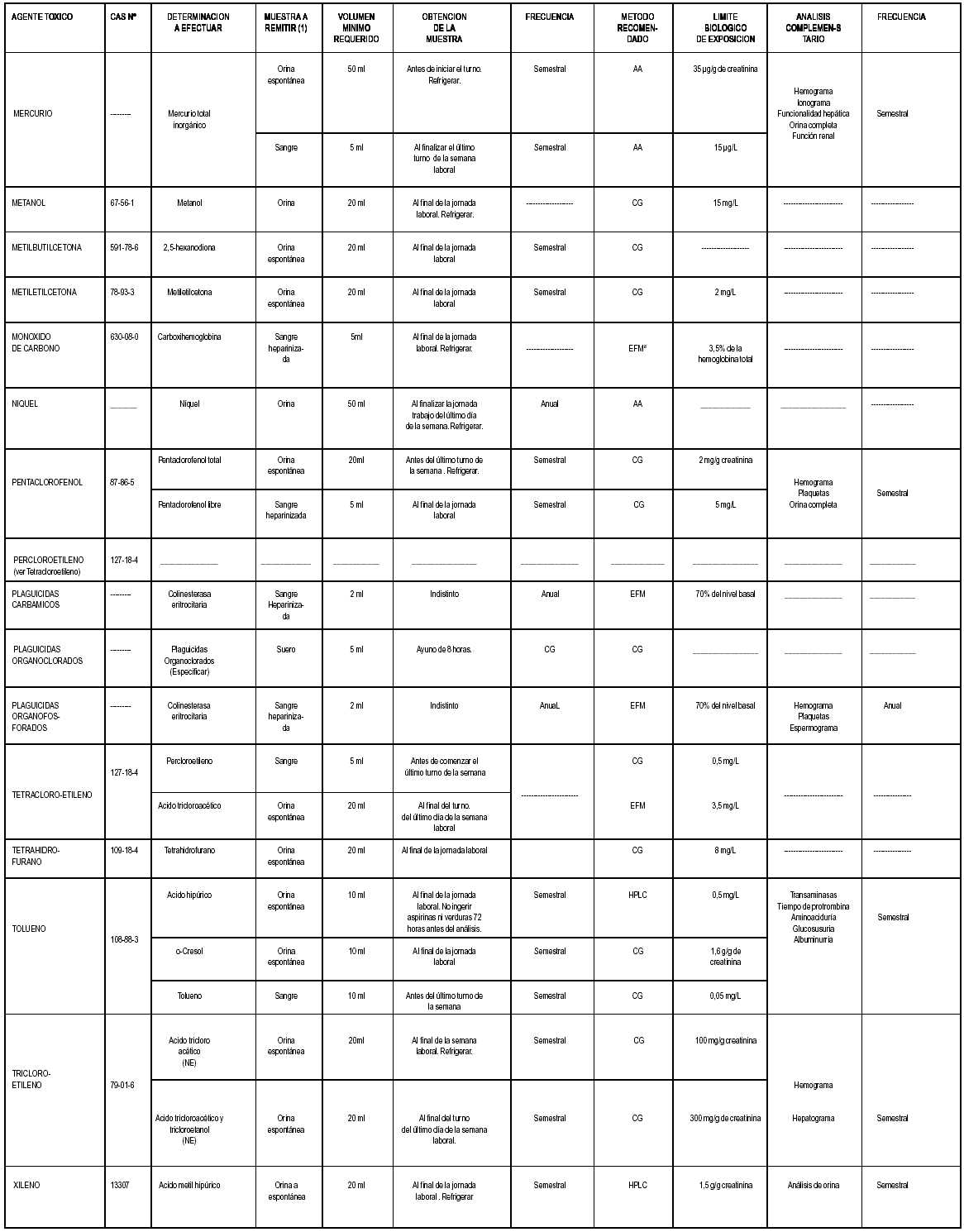
GUÍA PARA LA OBTENCIÓN, TRANSPORTE, CONSERVACIÓN Y ANÁLISIS DE MUESTRAS EN PACIENTES CON PROBABLE INTOXICACIÓN CRÓNICA
Bibliografía: -ACGIH. "TLVs and BEIs", 2001 -Albiano, Nelson . "Toxicología Laboral. Criterios para la Vigilancia de los Trabajadores Expuestos a Sustancias Químicas". Editorial Polemos, 1999. -Sullivan, J. ; Krieger, G. "Clinical Environmental Health and Toxic Exposures". 2da. Edición. Editorial: Lippincott Williams and Wilkins, 2001. -Lauwerys, R. "Toxicología Industrial e Intoxicaciones Profesionales". Editorial Masson, 1994.
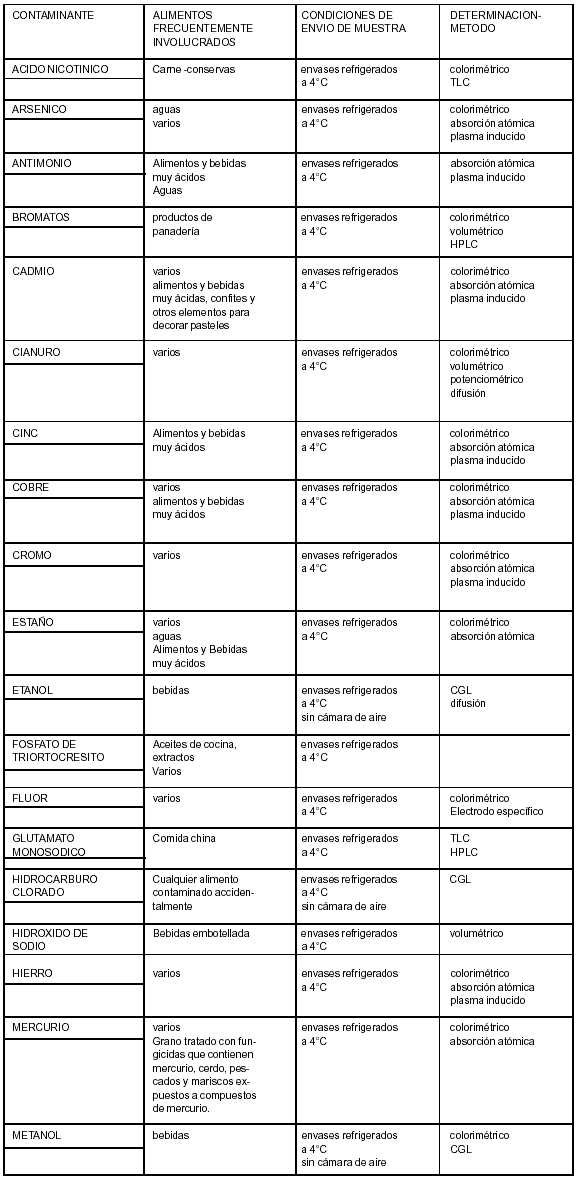
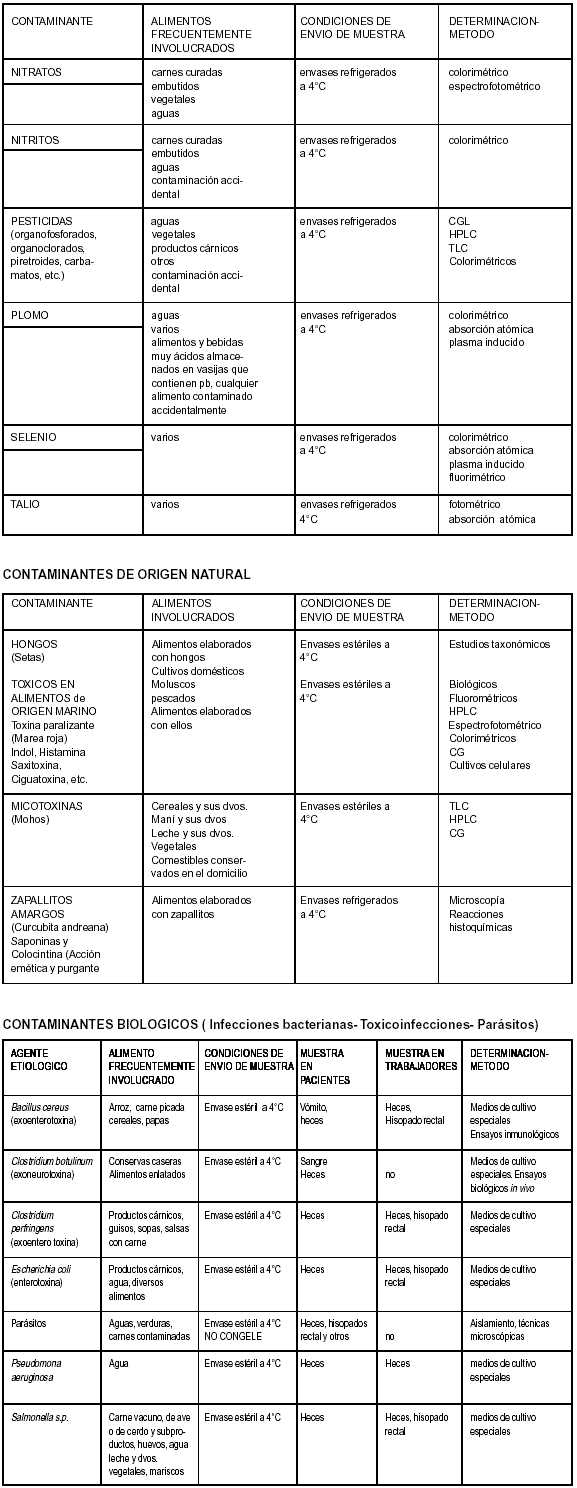
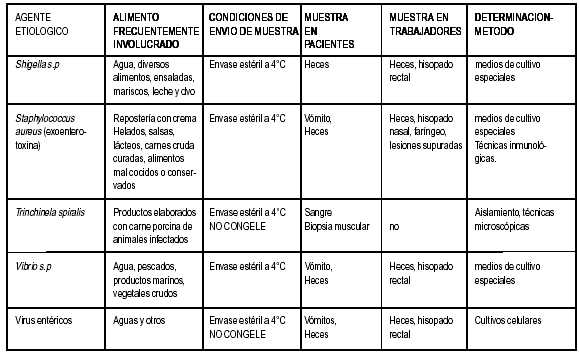
GUIA PARA LA OBTENCION, TRANSPORTE CONSERVACION Y ANALISIS DE MUESTRAS DE PACIENTES CON PROBABLE INTOXICACION POR ALIMENTOS
CONTAMINANTES QUIMICOS - ADITIVOS ALIMENTARIOS TOXICOS FORMADOS DURANTE LA ELABORACION
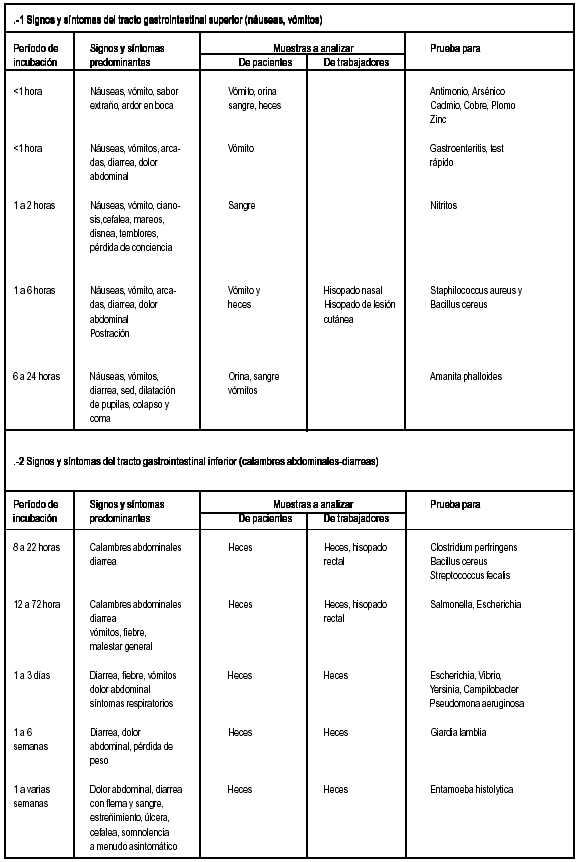
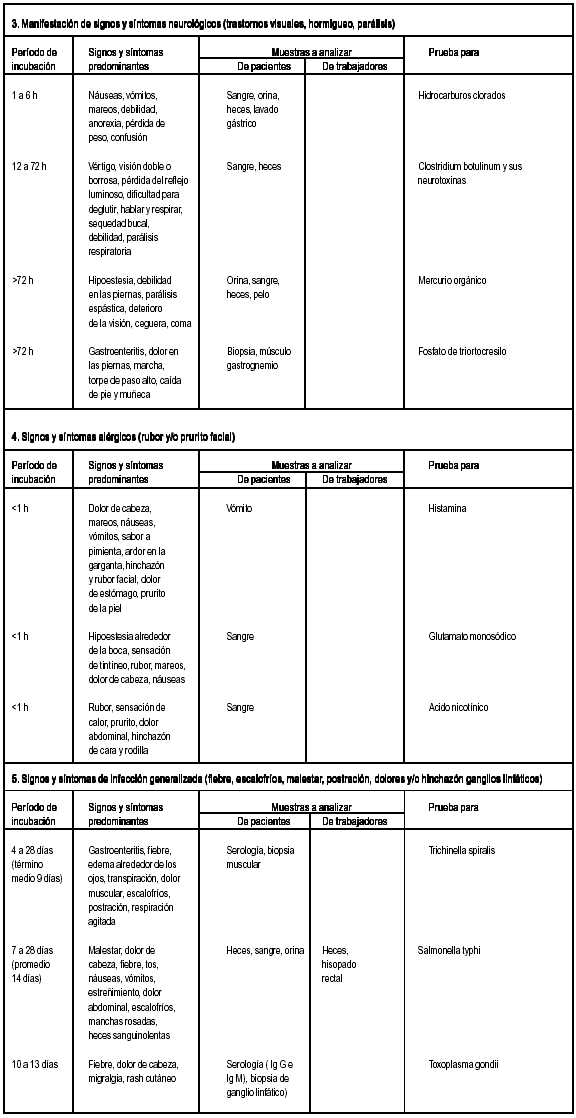
REMISION DE MUESTRAS AL LABORATORIO Las muestras para el Laboratorio deberán colocarse en envases limpios e inertes que eviten todo tipo de contaminación externa. Para estudios bacteriológicos deberán ser estériles. El envase deberá cerrarse herméticamente de tal manera que pueda detectarse cualquier apertura no autorizada y se deberá enviar al Laboratorio lo antes posible, adoptando todas las precauciones para evitar derrames y deterioro del material. Los alimentos congelados deberán ser mantenidos como tales y las muestras fácilmente putrescibles deberán mantenerse a 4°C o congeladas en los casos que se permitan. Las muestras deberán estar identificadas y acompañadas de los protocolos de envío de muestras y cadena de custodia debidamente completadas. GUIA PARA TOMA DE MUESTRAS Y PRUEBAS DE LABORATORIO EN PACIENTES CON PROBABLE INTOXICACION ALIMENTARIA DE ACUERDO A SIGNOS - SINTOMAS Y PERIODO DE INCUBACION
REFERENCIAS BIBLIOGRAFICAS CAA CODIGO ALIMENTARIO ARGENTINO Ley 18284, Norma Mercosur y Norma FIL C 50/95 Codex Alimentarius CCFAC: Comité del Codex sobre aditivos alimentarios y contaminantes de los alimentos METODOS NORMATIZADOS PARA EL ANALISIS DE AGUAS- APHA-AWWA-WPCF AOAC Official Methods of Analisis of the Association of Official Analytical CHEMISTS (Ultima edición) NORMAS IRAM Nº 15: Establece criterio de muestreo, por tamaño, por costo. Criterios de muestra única con rechazo. Define lote. AQL: nivel aceptable de rechazo para microbiología de patógenos = a cero PRONAPAL Ministerio de Salud simil Pcia. de Buenos Aires GUIA VETA. INPPAZ/OPS. 1996.
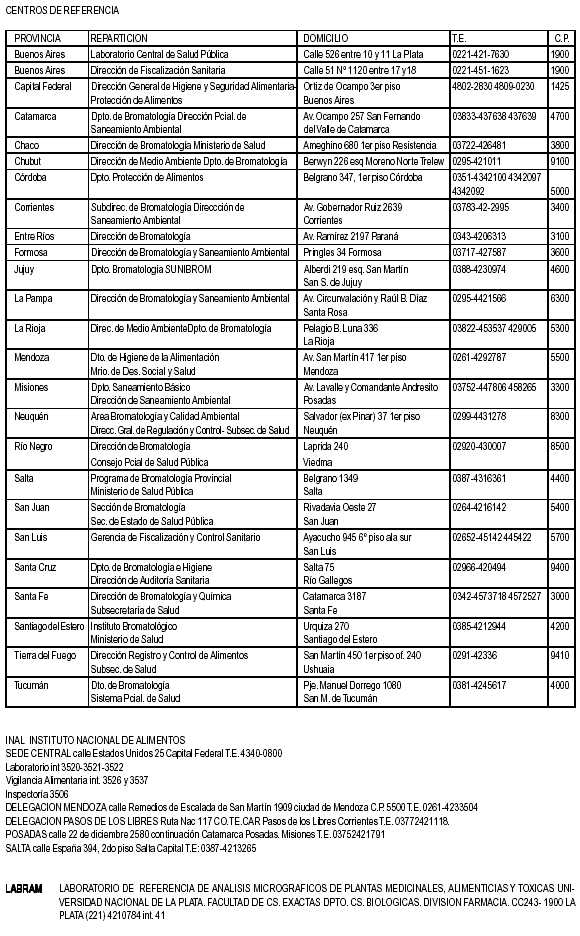
LABORATORIOS DE ANALISIS CLINICOS TOXICOLOGICOS DE LA REPUBLICA ARGENTINA DIRECTORIO DE LABORATORIOS DE ANALISIS CLINICOS TOXICOLOGICOS DE LA REPUBLICA ARGENTINA (según su ubicación geográfica) CAPITAL FEDERAL CENATOXA (CENTRO DE ASESORAMIENTO TOXICOLOGICO ANALITICO) – Cátedra de Toxicología y Química Legal – Fac. de Farmacia y Bioquímica – Univ. de Buenos Aires Responsable: Dra. Edda Villamil Junín 956 - 7º Piso - CP 1113 – Capital Federal Tel / Fax: (011) 4964-8283 / 84 E-mail: cenatoxa@ffyb.uba.ar / evillaam@ffyb.uba.ar LABORATORIO DIVISION TOXICOLOGICA - Hospital Escuela "José de San Martín" - Universidad de Buenos Aires Responsable: Dra. Isabel YohenaAvda Córdoba 2331 - CP 1120 – Capital Federal Tel / Fax (011) 4508-3760 E-mail: dajae@arnet.com.ar LABORATORIO CENTRAL - Hospital de Pediatría "Juan P. Garrahan" Coordinadora: Dra. Sofía Liapchuc Responsable Toxicología: Dra. Marta Rubinstein Combate de los Pozos 1881- CP 1245 – Capital Federal Tel: (011) 4308-4300 Int.1264 / 65 Fax 4308-5325 E-mail mrubinstein@garra.giga.com.ar CENTRO DE INVESTIGACIONES TOXICOLOGICAS S.A. Responsable: Dr. Carlos A. Gotelli Avda. San Pedrito 220 - CP 1406 – Capital Federal Tel: (011) 4612-6912 / 4613-1100 Fax 4613-3707 E-mail postmaster@ciqe.sid.ar/dgotelli@impsatl.com.ar www.ciquime.org.ar LABORATORIO BIOMEDICO DR. RAPELA Responsable: Dr. Juan C. Rapela Ramón L. Falcón 2534 – Cap. Fed. Tel / Fax: (011) 4611 8479 – 46131984 e-mail: jcrapela@lab-rapela.com.ar Página Web: www.lab-rapela.com.ar GRUPO SERVICIOS Y ASISTENCIA TECNICA ANALITICA - Unidad de Actividad Química – Comisión Nacional de Energía Atómica Responsable: Lic. Roberto E. Servant Avda. Del Libertador 8250 – CP 1429 – Capital Federal Tel: (011) 4704-1317 Fax 4704-1190 E-mail servquim@cnea.gov.ar / pastore@cnea.gov.ar DEPARTAMENTO QUIMICO - Dirección de Pericias de Gendarmería Nacional Responsable: Comandante Principal Dr. Mario A. Galia Comandante Florencio O. Caballero Avda. Antártida Argentina 2258 – CP 1104 – Capital Federal Tel: (011) 4310-2641 Fax 4310-2772 E-mail sec.delitos.inform@impsat1.com.ar PROVINCIA DE BUENOS AIRES Haedo Norte MONITOREO DE DROGAS – Sección Química –Laboratorio Central Hospital Nacional Prof. A. Posadas Responsable: Dr.Jorge Ortiz Avdas. Illia y Marconi - Villa Sarmiento - CP 1706 - Haedo Tel: (011) 4469-9200 o 9300 interno 1175 Fax: int 1993 E-mail: estelasrodriguez@yahoo.com Lomas de Zamora BIOTOX - LABORATORIO DE ANALISIS CLINICOS Y TOXICOLOGICOS DEPARTAMENTO DE TOXICOLOGIA Y BROMATOLOGIA Responsable: Dr. Juan Carlos Alsamora Molina Arrotea 2124 – CP 1832 - Lomas de Zamora - Buenos Aires Tel / Fax: (011) 4283-0133 / 3131 E-mail: alsamora@ba.net La Plata LABORATORIO CENTRAL - Hospital Interzonal de Agudos Especializado en Pediatría "Sor Maria Ludovica" Responsable: Dra. Susana Jorge Calle 14, Nro.1631 - CP1900 – La Plata Tel: (0221) 457-5154 interno 1731 E-mail: bludovica_sap@hotmail.com CATEDRA DE TOXICOLOGIA Y QUIMICA LEGAL - Facultad de Ciencias Exactas - Universidad Nacional de La Plata Responsable: Dra. Leda Gianuzzi Calle 47 y 115 - CP 1900 – La Plata Tel: (0221) 421-0784 Interno 46 Fax 422-3409 E-mail: leda@nahuel.biol.unlp.edu.ar LABORATORIO DE TOXICOLOGIA Y QUIMICA LEGAL - Dirección General de Asesorías Periciales - Suprema Corte de Justicia de la Provincia de Buenos Aires Responsable: Dr. Luis A. Ferrari Calle 41 e/119 y 120 – CP 1900 – La Plata Tel: (0221) 422-8001 / 422-5011 Fax 422-9105 E-mail: ferrariluis@federal.com.ar Tandil LABORATORIO DE TOXICOLOGIA (SNITV) - Facultad de Veterinaria- Universidad Nacional del Centro de la Provincia de Buenos Aires Responsable: Dr. Alejandro Soraci - Dra. Ofelia Tapia Paraje Arroyo Seco s/n - Campus Universitario - CP 7000 - Tandil Tel: (02293) 42-2357 Fax 42-6667 E-mail: snitv@vet.unicen.edu.ar CORDOBA LABORATORIO HOSPITAL DE URGENCIAS Responsable: Dra. Susana Molina Barrios Catamarca 441 - CP 5000 - Córdoba Tel: (0351) 421-7037 / 433-2740 Fax 421-7004 E-mail: hospurg@tecomnet.com.ar LABORATORIO DE INVESTIGACIONES PSICONEUROFARMACOLOGICAS Y TOXICOLOGICAS PROF.L.S.MORRA Responsable: Dr. Cristian Hansen Avda. Sagrada Familia y Nazareth 3º - CP 5000 - Córdoba Tel: (0351) 481-3774 / 482-2191 Fax 481-8335 E-mail morracba@agora.com.ar AREA TOXICOLOGIA - Laboratorio Central – Hospital de Niños de la Santísima Trinidad Responsable: Dra. Graciela Suti Bajada Pucará– CP 5000 – Córdoba Tel: 0351-458-6400 E-mail: rafaelbuteler@yahoo.com.ar LABORATORIO DE QUIMICA ANALITICA – Agencia Córdoba Ciencia- Unidad CEPROCOR Responsables: Plaguicidas: Dra. Mirtha Nassetta, Metales Pesados: Dr. Raúl Badini, Medicamentos: Dra. Viviana Dabbene Alvarez de Arenales 230 – Barrio Juniors – CP 5000 – Córdoba Tel: (03541) 48-9650 / 51 / 52 / 53 Fax int. 129 E-mail: mnassetta@cordoba.com.ar / rbadini@cordoba.com.ar / vdabbene@cordoba.com.ar JUJUY LABORATORIO CENTRAL DE SALUD PUBLICA – Dirección Provincial de Sanidad Responsable: Dra. Sara R. Barberis Alberdi 219 - CP 4600 – San Salvador de Jujuy Tel: (0388) 422-1308 Fax 422-1239 E-mail: celabjujuy@arnet.com.ar LABORATORIO INQA (Investigación Química Aplicada) – Programa: Detección de Residuos de Plaguicidas - Facultad de Ingeniería - Universidad Nacional de Jujuy Responsable: Graciela Bovi Mitre Gorriti 237- CP 4600 - San Salvador de Jujuy - Jujuy Tel: (0388) 422 1581 E-mail gbovi@imagine.com.ar MISIONES LABORATORIO DE TOXICOLOGIA Y QUIMICA LEGAL - Facultad de Ciencias Exactas, Químicas y Naturales - Universidad Nacional de Misiones Responsable: Dr. Carlos O. González López Torres y Moreno - CP 3300 - Posadas Tel / Fax (03752) 42-7687 E-mail: carlos@escenf.unam.edu.ar / cgonzalez@novell.unam.edu.ar SALTA SERVICIO DE TOXICOLOGIA - Hospital Materno-Infantil Responsable: Dra. Bettina S. Valle Avda. Sarmiento 625 – CP 4400 - Salta Tel: (0387) 421-3954 - interno 115 Fax 422-0519 E-mail: bevalle@sinectis.com.ar SAN LUIS CATEDRA DE TOXICOLOGIA Y QUIMICA LEGAL - Facultad de Química, Bioquímica y Farmacia - Universidad Nacional de San Luis Responsable: Dra. Diana González de Cid Chacabuco y Pedernera – CP 5700 – San Luis Tel: (02652) 42-3789 - interno 112 Fax 43-1301 E-mail: dgonza@unsl.edu.ar SANTA FE Rosario INSTITUTO DE BIOQUIMICA CLINICA (IBC) Responsables: Dres Scrigna J., Solari M., Pugliessi H. San Juan 1768 -Rosario (S2000BED) Tel/Fax (54-341) 426-0423 / 440-5772 / 421-9127 E-mail: gscrigna@elsitio.net TOXICOLOGIA INTEGRAL ARGENTINA S.A. (TIASA) Responsable: Dr. Daniel C. Ezpeleta 3 de Febrero 1649 - CP 2000 - Rosario Tel: (0341) 448-6541 Fax 482-3262 E-mail: tiasa@cablenet.com.ar LABORATORIO DE TOXICOLOGIA APLICADA - Facultad de Ciencias Bioquímicas – Universidad Nacional de Rosario Responsable: Dr. Héctor R. Girolami Suipacha 531/570 - CP 2000 - Rosario Tel: (0341) 480-4593 / 98 interno 237 Fax 480-4597 / 8 E-mail: julialab@satlink.com INSTITUTO DE ESTUDIOS BIOQUIMICOS (IDEB) Responsable: Dr. Carlos A. García Mendoza 1180 – CP 2000 – Rosario Tel: (0341) 424-9962 / 421-8296 Fax 424-9810 / 421-8296 E-mail: caralb@ideb.org.ar Santa Fe SECCION TOXICOLOGIA - Hospital Provincial José M. Cullen Responsable: Dra. Elisa C.K. de Kaczan Avda. Freyre 2150 - CP 3000 – Santa Fe Tel: (0342) 459-8770 / 459-8336 E-mail: hospjmc@ssdfe.com.ar CATEDRA DE TOXICOLOGIA, FARMACOLOGIA Y QUIMICA LEGAL - Facultad de Bioquímica y Ciencias Biológicas - Universidad Nacional del Litoral Responsable: Dra. Elisa C. K. de Kaczan Ciudad Universitaria – Paraje el Pozo - CP 3000 – Santa Fe Tel: (0342) 457-1138 / 1 E-mail ekaczan@fbcb.unl.edu.ar DEPARTAMENTO DE TOXICOLOGIA - Laboratorio Integral Responsable: Dra. Gabriela Fiorenza Balcarce 1615 – CP 3000 – Santa Fe Tel: (0342) 455-3203 Fax. (0342) 456 5537 E-mail: integralsa@infovia.com.ar CENTER LAB Responsable: Carlos Chichizola San Lorenzo 2780 – CP S3000EUL - Santa Fe – Santa Fe Te/Fax: (0342) 455-1615 / 456-2117 e-mail: clab@arnet.com.ar TUCUMAN LABORATORIO DE TOXICOLOGIA - Dirección de Salud Municipal Responsable: Bqca. Marta E. Peñaloza de Terán Chacabuco 239 P.1- CP 4000 – San Miguel de Tucumán Tel: (0381) 421-2329 / 421-2224 E-mail: teranpena@infovia.com.ar LABORATORIO DE TOXICOLOGIA – Cuerpo Médico Forense del Poder Judicial de Tucumán Responsable: Bqca. Sara Cristina Daives Avda. Independencia 990 – CP 4000 – San Miguel de Tucumán Tel: (0381) 429-1512 E-mail: cridaives@tucbbs.com.ar / cristinadaives@hotmail.com LABORATORIO TOXICOLOGICO – (LABOTOX) Responsable: Bqca. Carolina S. Albornoz Piossek de Ponce de León Lamadrid 667 – CP 4000 – San Miguel de Tucumán Tel / Fax: (0381) 424-8866 E-mail: suaponce@ciudad.com.ar |
|
-o- |