|
| |
|
Argentina,
Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) |
|
- modifica y/o
complementa a: ley 16463,
ley 18284,
decreto 1490/92 PEN,
decreto 772/15 PEN.
- modificada y/o
complementada por: |
Administración Nacional de Medicamentos,
Alimentos y Tecnología Médica
ANMAT -
IMPORTACION, EXPORTACION,
PRODUCCION, ELABORACION, FRACCIONAMIENTO, COMERCIALIZACION
Y/O DEPOSITO
Disposición (ANMAT) 7771/15. Del
23/9/2015. B.O.: 29/9/2015. ANMAT. Persona física y/o jurídica que
realice importación, exportación, producción, elaboración,
fraccionamiento, comercialización y/o depósito, en jurisdicción
nacional o con destino al comercio interprovincial, de las
sustancias incluidas en el Anexo I de la presente disposición,
empleadas en medicina y cosmética humanas y en productos de uso
doméstico. Obligaciones.
Bs. As., 23/09/2015
VISTO las Leyes 16.463 y 23.737, el Decreto N° 772/15, el Decreto N°
1490/92 y el Expediente N° 1-0047-0000-010463-15-3 del Registro de
esta ADMINISTRACIÓN NACIONAL DE MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA
MÉDICA (ANMAT); y
CONSIDERANDO:
Que por Resolución N°
580/14 de la SECRETARÍA DE PROGRAMACIÓN PARA LA PREVENCIÓN DE LA
DROGADICCIÓN Y LA LUCHA CONTRA EL NARCOTRÁFICO DE LA PRESIDENCIA DE
LA NACIÓN (SEDRONAR) se aprobó el Código Voluntario de Conducta
Responsable respecto del Uso de Precursores Químicos.
Que de
acuerdo con lo señalado en el referido Código existen ciertas
sustancias lícitas que, si bien no son precursores químicos conforme
lo establece el Anexo I del Decreto N° 1095/96, modificado por el
Decreto N° 1161/00, ni estupefacientes conforme el Decreto N°
299/10, modificado por el Decreto N° 772/15, deben ser tenidas en
cuenta por los operadores, toda vez que pueden encontrarse
relacionadas con la elaboración ilícita de estupefacientes.
Que algunas de estas sustancias son las denominadas sustancias de
corte, utilizadas para “estirar” el producto final, obteniendo más
dosis de menor calidad y de este modo lograr un rédito económico
mayor.
Que entre estas sustancias de corte o estiramiento se
encuentran ingredientes farmacéuticos activos (IFAs) tales como la
lidocaína, benzocaína, paracetamol, ibuprofeno, cafeína y levamisol
y excipientes como el Manitol y la lactosa, de uso en el campo de
las industrias farmacéutica, cosmética y de productos de uso
doméstico.
Que algunas de estas sustancias, tales como el
manitol, la lactosa y la cafeína, se utilizan también en la
industria alimenticia.
Que en la Jornada de capacitación de
inspectores llevada adelante en conjunto con la SEDRONAR el 18 de
septiembre de 2014, la Secretaría planteó la problemática respecto
de la fiscalización de las referidas sustancias del corte para lo
cual se ve limitada por no tratarse de precursores químicos, no
obstante lo cual fueron incluidas en el listado provisional de
control voluntario obra ante en el mencionado Código Voluntario de
Conducta Responsable respecto del Uso de Precursores Químicos.
Que en dicha oportunidad la Dirección de Vigilancia de
Sustancias Sujetas a Control Especial del INSTITUTO NACIONAL DE
MEDICAMENTOS (INAME) se comprometió a evaluar la situación y a
comunicar la información obtenida al respecto.
Que el Decreto
Nº 1490/92, de creación de esta Administración Nacional, declaró de
interés nacional las acciones dirigidas a la prevención, resguardo y
atención de la salud de la población que se desarrollen a través del
control y fiscalización de la calidad y sanidad de los productos,
sustancias, elementos y materiales que se consumen o utilizan en la
medicina, alimentación y cosmética humanas, y del contralor de las
actividades, procesos y tecnologías que mediaren o estuvieren
comprendidos en dichas materias.
Que en virtud del artículo
3º inciso a) del mencionado decreto, esta Administración Nacional
tiene competencia en todo lo referente al control y fiscalización
sobre la sanidad y la calidad de las drogas, productos químicos,
reactivos, formas farmacéuticas, medicamentos, elementos de
diagnóstico, materiales y todo otro producto de uso y aplicación en
medicina humana.
Que los incisos b) y c) otorgan competencia
a este organismo, respectivamente, en el control y fiscalización
sobre la sanidad y calidad de los alimentos acondicionados,
incluyendo los insumos específicos, aditivos, colorantes,
edulcorantes e ingredientes utilizados en la alimentación humana y
de los materiales en contacto con los alimentos como también de los
productos de uso doméstico y en el control y fiscalización sobre la
sanidad y calidad de los productos de higiene, tocador y cosmética
humana y de las drogas y materias primas que los componen.
Que por otra parte, de acuerdo con el inciso e) corresponde a esta
Administración Nacional el contralor de las actividades, procesos y
tecnologías que se realicen en función del aprovisionamiento,
producción, elaboración, fraccionamiento, importación y/o
exportación, depósito y comercialización de los productos,
substancias, elementos y materiales consumidos o utilizados en la
medicina, alimentación y cosmética humanas.
Que asimismo, de
conformidad con el inciso f) del referido artículo 3°, corresponde a
la ANMAT la realización de acciones de prevención y protección de la
salud de la población, que se encuadren en las materias sometidas a
su competencia.
Que finalmente, según el inciso g) del
artículo 3° citado, es competencia de esta Administración toda otra
acción que contribuya al logro de los objetivos establecidos en el
artículo 1º del Decreto Nº 1490/92.
Que de conformidad con
las atribuciones que le fueran asignadas a esta Administración
Nacional resulta oportuno reforzar las medidas de control y
fiscalización de los mencionados IFAs y excipientes a los efectos de
limitar la posibilidad de desvío y/o uso ilícito de estas
sustancias, contribuyendo de esta manera a la prevención y
protección de la salud de la población.
Que el Instituto
Nacional de Medicamentos, la Dirección de Vigilancia de Productos
para la Salud, el Instituto Nacional de Alimentos y la Dirección
General de Asuntos Jurídicos han tomado la intervención de su
competencia.
Que se actúa en virtud de las facultades
conferidas por los Decretos N° 1490/92 y 1886/14.
Por ello,
EL ADMINISTRADOR NACIONAL DE LA ADMINISTRACIÓN NACIONAL DE
MEDICAMENTOS, ALIMENTOS Y TECNOLOGÍA MÉDICA
DISPONE:
ARTÍCULO 1° — Establécese que toda persona física y/o jurídica que
realice importación, exportación, producción, elaboración,
fraccionamiento, comercialización y/o depósito, en jurisdicción
nacional o con destino al comercio interprovincial, de las
sustancias incluidas en el Anexo I de la presente disposición,
empleadas en medicina y cosmética humanas y en productos de uso
doméstico, deberá:
1. Inscribirse ante la Dirección de
Vigilancia de Sustancias Sujetas a Control Especial del INSTITUTO
NACIONAL DE MEDICAMENTOS (INAME), mediante la presentación de la
declaración jurada que, como Anexo II, forma parte integrante de la
presente disposición.
Los sujetos que no se encuentren
previamente inscriptos ante la referida Dirección deberán presentar,
adicionalmente, la documentación respaldatoria que se indica en
dicho Anexo.
La renovación de la inscripción será anual.
2. Llevar registro fiel de los movimientos de stock y
distribución primaria de las sustancias incluidas en el Anexo I de
la presente disposición.
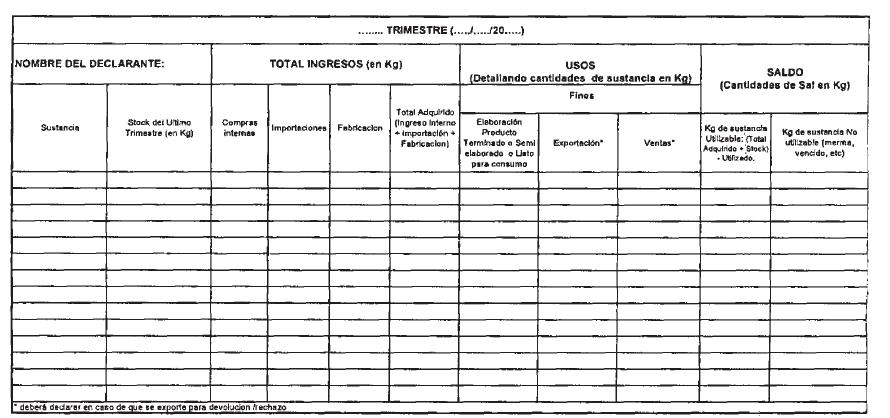
3. Presentar informes trimestrales
de movimiento de stock conforme el formulario que, como Anexo III,
forma parte integrante de la presente disposición.
ARTÍCULO
2° — Establécese que toda persona física y/o jurídica que realice
importación y exportación de las sustancias incluidas en el Anexo I
de la presente disposición, empleadas en alimentación humana, deberá
dar cumplimiento con lo establecido en el artículo 1°.
ARTÍCULO 3° — El incumplimiento de lo dispuesto en la presente
disposición hará pasible a los infractores de las sanciones
previstas en las Leyes 16.463 y 18.284 y el Decreto N° 341/92, sin
perjuicio de las demás acciones que pudieran corresponder.
ARTÍCULO 4° — Invítase a los gobiernos de las provincias y de la
Ciudad Autónoma de Buenos Aires, en el marco de ANMAT Federal, a
adherir a la presente disposición.
ARTÍCULO 5° — Regístrese.
Dése a la Dirección Nacional del Registro Oficial para su
publicación. Comuníquese a las Cámaras y entidades profesionales de
los sectores involucrados. Cumplido, archívese.
- Manitol
- Lidocaína
-
Benzocaina
- Cafeína
- Lactosa
- Levamisol
- Paracetamol
- Ibuprofeno
ANEXO II


ANEXO III DISPOSICIÓN N°
|
|
-o-
arriba |
|